成体干细胞存在于大多数哺乳动物的组织和器官中,是维持正常机体内环境和组织修复不可缺少的成分。随着年龄的增长,组织特异性的干细胞和干细胞池的改变引起衰老组织持续性的自稳和再生能力的下降,理解干细胞功能衰退的分子途径有助于开发衰老性疾病的新疗法。
1.活性氧类(Ros)
1972年,Harman教授提出衰老的氧自由基理论,强调衰老导致的细胞损伤和线粒体功能减退引起ROS产生增加,反过来进一步加剧细胞大分子和线粒体的破坏、细胞裂解。有人提出假设,ROS促进干细胞衰老。研究表明,衰老的间充质干细胞(MSCs)内ROS水平升高。此外小鼠的造血干细胞(HSCs)和神经干细胞(NSCs)中增高的ROS表达导致细胞增殖异常、肿瘤样改变以及干细胞的自我复制能力下降。
2.DNA损伤
引起衰老干细胞中损伤DNA累积的原因很多,譬如,长时间的破坏、损伤概率增加和修复能力下降等。DNA损伤可诱发缺陷细胞的产生、干细胞衰退或肿瘤性化生,以及干细胞自我复制和分化能力的改变,呈现年龄相关性的器官功能和机体稳态的丧失。
3.蛋白质稳态改变
蛋白质稳态的缺陷导致损伤蛋白质的异常折叠、毒性蛋白质聚积,引起细胞损伤和组织功能失调。蛋白质稳态是维持干细胞的重要决定因素,自噬相关基因7(Atg7)缺乏的HSCs中ROS水平增加和HSC被清除,而Atg8过表达增加果蝇的寿命。另一项研究表明,FoxO3A引发的自噬功能保护HSCs免除衰老相关自由基引起的损伤。mTOR引起自噬蛋白的抑制,应用雷帕霉素(mTOR抑制剂)能够恢复衰老HSCs的自我复制和造血重建功能。蛋白质稳态是维持人胚胎干细胞的基本因素,然而其与干细胞衰老的直接关系尚未明确。
4.线粒体功能失调
研究表明,线粒体DNA点突变和缺失的增加,伴随着寿命缩短和早衰。除了线粒体DNA的突变,年龄相关的细胞和代谢改变进一步引起线粒体改变和影响衰老过程。营养和能量平衡与线粒体的功能和寿命有关。在HSCs中,随着年龄的增长,衰老HSCs营养摄取能力下降,提示营养传感途径涉及干细胞的衰老过程。相反,增强的线粒体功能伴随着干细胞功能和组织再生能力的提高,譬如,短期限制热量摄入能够增加线粒体的容积和促进氧化代谢的能力,在年轻和老龄鼠内观察到骨骼肌干细胞的储备和功能增加。
5.干细胞缺失和衰退
在骨骼肌、神经和生殖干细胞中均发现年龄相关的干细胞数量减少或细胞周期紊乱,可能与干细胞丧失自我复制和分化能力,或应激引起的干细胞凋亡或衰退相关。研究发现,干细胞衰竭也可能与细胞静态和增殖之间的失衡有关,过度增殖加速干细胞衰竭。此外,细胞内的ROS水平决定HSCs及其他成体干细胞的静止和增殖间平衡,低水平ROS维持干细胞静态,ROS过多引起细胞增殖和分化。譬如,进行性杜氏肌肉营养不良症中持续性的肌肉纤维变性引发骨骼肌干细胞不断再生,消耗干细胞的再生能力。

6.细胞微环境
干细胞壁龛提供特殊的微环境,维持干细胞数量并调节其功能,壁龛细胞衰老和壁龛内非细胞成分的改变可引起干细胞功能的改变。譬如,帽细胞和中心细胞是生殖干细胞(睾丸和卵巢)的支持细胞,随着年龄的增长,细胞数量减少,削弱了维持干细胞相关的骨形成蛋白信号。此外,衰老引起循环中各种因子的改变,广泛影响组织干细胞。老龄鼠中,转化生长因子 β在骨骼肌中的累积阻碍了肌肉再生和卫星细胞的增殖。研究证实,通过共生的原理,将年老的骨骼肌置于年轻动物的体循环中,能够促进老化肌肉中的骨骼肌卫星细胞激活。应用同样的方法,发现老龄鼠神经再生率增加、髓鞘再生和中枢神经系统功能改善。可见衰老的机体内环境明显影响衰老干细胞和非干细胞的表型。
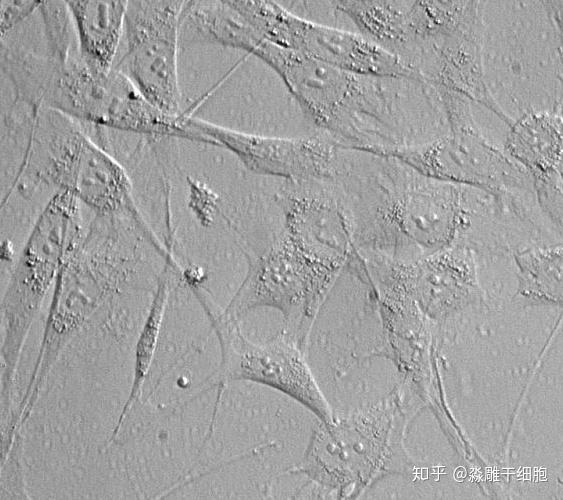
7.表观遗传学改变
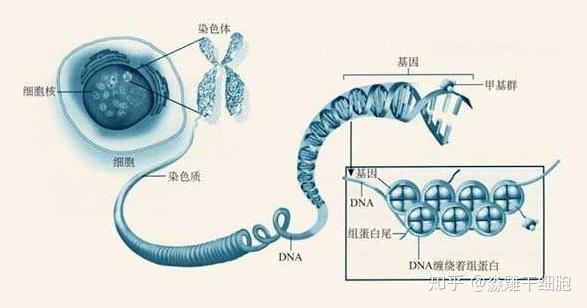
研究表明,表观遗传调控在干细胞功能调节中很重要,衰老时表观基因组的改变影响干细胞的衰老进程。譬如,衰老HSCs的基因组中,与细胞分化有关的特异性DNA甲基化位点增加和组蛋白修饰异常,与HSCs自我复制相关基因的表达改变。毛囊干细胞中,DNA甲基转移酶1的缺少导致干细胞衰竭,呈现极端老化的毛囊和皮肤表型。





 设为首页◇加入收藏
设为首页◇加入收藏  联系我们
联系我们


 关注官方微信
关注官方微信